
2025-10-31 07:07:26
近年來,AAV在cancer疾病的醫治中顯示出巨大的價值。AAV作為基因藥物的載體已在肺、肝、眼、腦、肌肉等多個臨床試驗(超過100次)中得到應用,并在盲癥和血友病方面取得了巨大成功。2012年,AAV1載體編碼的脂蛋白脂肪酶成為歐盟批準的shou個用于醫治脂蛋白脂肪酶缺乏癥的基因產物(Glybera)。5年后,另一種AAV介導的基因藥物(Luxturna)隨后獲準在美國上市。基于AAV9的基因療(Zolgensma)也被用于醫治脊髓性肌肉萎縮。腺病毒在基礎和實驗研究有這么強的生命力原因在于:宿主范圍廣,對人致病率低;腺病毒粒子相對穩定,病毒基因重排頻率低;**性高,不整合到染色體中,無插入致病基因,不干擾其他宿主基因。ArcticZymes Technologies成立于20世紀80年代后期,總部位于挪威北部的特羅姆瑟(Troms?)。浙江高鹽核酸酶哪家公司銷售
ArcticZymes Technologies有兩條產品線,分別針對分子診斷和生物藥物生產兩個領域。在分子診斷領域,產品有蝦堿酶(SAP)、UNG酶、等溫擴增酶(IsoPol)、連接酶、蛋白酶、內切核酸酶及外切核酸酶等,涉及核酸抽提、擴增及測序等應用。在生物藥物生產領域,全球創新的鹽活性核酸酶(Salt Active Nucleases, SANs)系列產品以其獨特優勢,在細胞基因藥物及RNA藥物生產中表現出更好的性能。其中,鹽活性核酸酶SANs系列產品包含兩款產品,分別是SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶;兩款酶的差別在于發揮酶活的鹽濃度范圍分別是生理鹽濃度范圍和400-600mM高鹽濃度范圍。湖北70921-202高鹽核酸酶江蘇高鹽核酸酶服務哪家好呢,歡迎咨詢上海倍篤生物 。

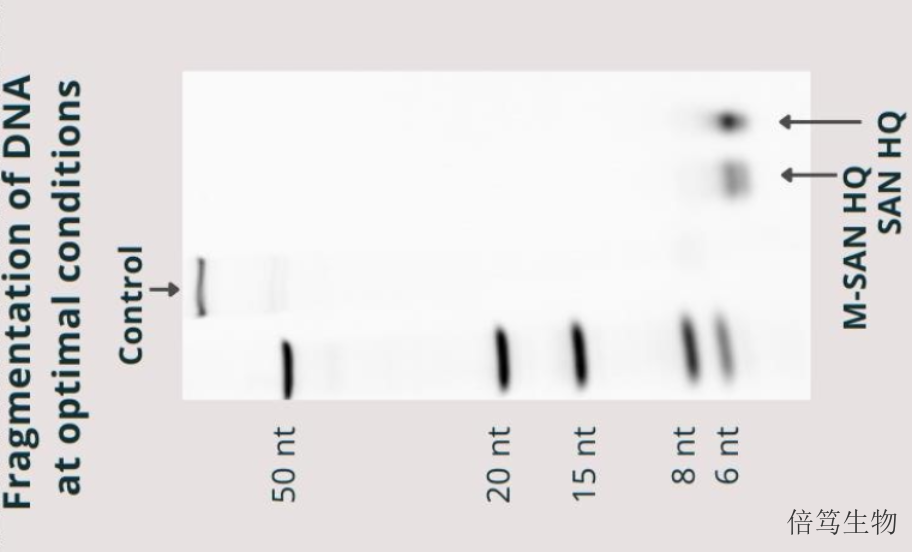
殘留的宿主DNA是生產中產生的雜質,其存在潛在的致瘤性、傳染性和免疫原性等風險。相關研究表明,基因的大小普遍在200bp以上,因此大于200bp有可能會有一定的致病性,而且殘留DNA片段越大,生物制品的風險等級越高。因此,各國監管機構對其提出了嚴格要求。美國食品藥品監督管理局(FDA)在《關于人類基因zhiliao新產品生產指導文件》中明確指出HCD的片段要小于200bp。2022年5月,**藥品監督管理局藥品評審中心(CDE)發布的《體內基因藥物產品藥學研究與評價技術指導原則(試行)》中也明確指出需對DNA殘留量和殘留片段大小進行控制,建議盡量將DNA殘留片段的大小控制在200bp以下。
經典的慢病毒載體(LV)的生產工藝如下,——三質粒系統瞬時轉染HEK293細胞系,轉染24小時后LV由轉染陽性細胞生產并排出到培養上清液中;收獲上清培養液后,加入核酸酶去除HCD污染,通過澄清步驟去除大的細胞碎片等雜質;下游純化步驟分離LV載體,純化方法包括切向流過濾TFF、色譜純化及超速離心;純化后的LV病毒顆粒經過無菌過濾,更換到優化后的配方中,灌裝并冷凍保存。每批Car-T生產時取對應量的LV病毒,切忌反復凍融,否則LV病毒會失活。南京高鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。
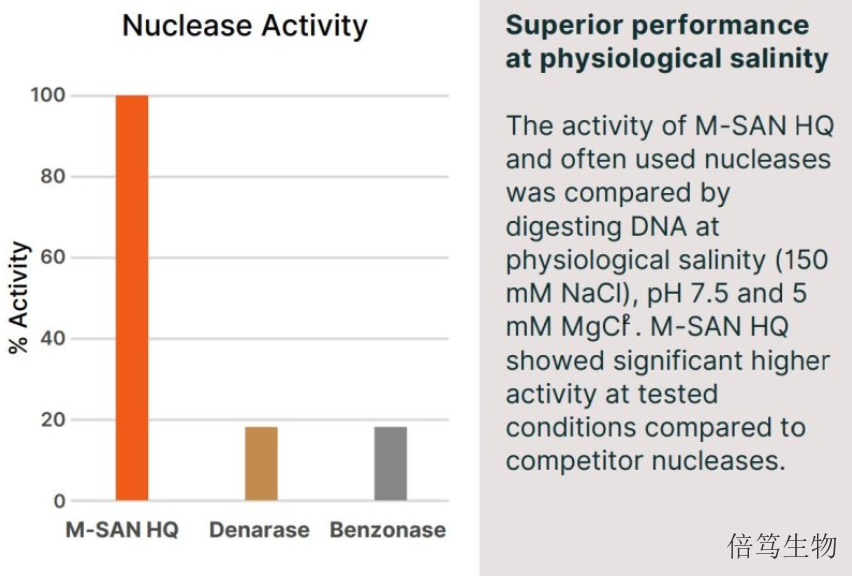
ArcticZymes Technologies成立于20世紀80年代后期,總部位于挪威北部的特羅姆瑟(Troms?)。在生物制品生產,如AAV載體及腺病毒載體疫苗生產中,宿主細胞DNA殘留是關鍵質量參數之一,高鹽濃度下,宿主DNA與蛋白質能夠更高效解離,從而更容易被降解。ArcticZymes廠家管控整個供應鏈及生產流程,協助客戶進行文件審計及現場審計。1.高鹽濃度下,宿主DNA與蛋白質能夠更高效解離,從而更容易被降解。在AAV生產過程中鹽濃度是純化工藝的重要參數之一,高鹽濃度能夠減少目標產物聚集、增加目標產物溶解度及提高目標產物產量。蘇州高鹽核酸酶哪家好呢,歡迎咨詢上海倍篤生物 。北京在線高鹽核酸酶聯系方式
浙江高鹽核酸酶款式哪家好呢,歡迎咨詢上海倍篤生物 。浙江高鹽核酸酶哪家公司銷售
上海倍篤生物科技有限公司(簡稱“倍篤生物”),由中國科學院及生物醫藥產業界人士,于2018年1月共同創立。公司代理多個品牌的儀器、試劑及耗材,遵守相關法規要求,如cGMP規范、ISO13485質量管理體系認證等,致力于為診斷領域如分子診斷及病原微生物檢測研發等,藥物研發領域如細胞基因藥物、核酸藥物、抗體藥物、干細胞及外泌體研究等客戶提供合規、高質量物料及專業服務,以期與客戶共同協作,加快研發及生產進度,為客戶提供更多價值。浙江高鹽核酸酶哪家公司銷售